La sperimentazione clinica è la metodologia che la scienza medica adotta per dimostrare l’efficacia di un farmaco in una determinata malattia. Tale metodologia prevede che, basandosi su informazioni certe (evidenze su cellule e animali), si facciano delle deduzioni sull’efficacia nell’uomo; deduzioni che andranno quindi verificate con protocolli sperimentali condotti secondo le linee guida internazionali[1]
Tutelare le persone malate arruolate nella sperimentazione è compito dei Comitati Etici (CE) che intervengono nel processo di autorizzazione dello studio clinico.
Il Decreto legislativo 2003/211 (attuazione della direttiva 2001/20/CE relativa all’applicazione della buona pratica clinica nell’esecuzione delle sperimentazioni cliniche di medicinali per uso clinico”[2]) stabilisce che
Prima di tutto il CE valuta se le fasi precliniche e gli studi su volontari sani abbiano fornito evidenze solide di sicurezza e indicazioni di efficacia nell’uomo. A seguire si procede con l’analisi del protocollo sperimentale; il CE deve assicurare ai pazienti che il protocollo sia disegnato in modo appropriato per fornire dati validi e robusti. E’ evidente che non sia etico sottoporre le persone malate ad un trattamento in uno studio metodologicamente carente e che per questo non potrà fornire evidenze, cioè prove solide e credibili.
Per capire meglio l’impatto del disegno sperimentale sulla validità dei dati, procediamo con esempi partendo dai gruppi di pazienti in studio.
Allo scopo di verificare l’efficacia del farmaco A è necessario il confronto o con il placebo, cioè una sostanza inerte (zucchero o acqua, per esempio), o con un farmaco B di cui già se ne conosce l’efficacia. Se l’uso del placebo è eticamente accettabile quando la malattia su cui si conduce la sperimentazione è orfana, cioè non dispone di alcuna terapia approvata, al contrario, quando la patologia ha opzioni terapeutiche valide, il paragone andrà condotto verso il farmaco già registrato ed efficace nella specifica malattia. Quindi, lo studio deve essere controllato o verso placebo o verso altro farmaco efficace.
Altro elemento cruciale del disegno è l’analisi statistica: essa permette sia di calcolare il numero minimo di pazienti da arruolare a garanzia della robustezza delle conclusioni sia di stabilire, con una determinata certezza, la relazione tra l’efficacia e il farmaco in studio.
Le persone coinvolte devono essere adeguatamente informate su tutto ciò che riguarda il farmaco sperimentale, le procedure dello studio, i potenziali rischi e benefici. Solo un adeguato approfondimento di questi aspetti garantisce la libera scelta del paziente e il CE vaglia se il modulo del consenso informato scritto sia appropriato allo scopo.
Il CE deve, cioè, verificare la fattibilità del protocollo in termini di correttezza scientifica e coerenza tra obiettivi (dimostrare l’efficacia) e mezzi (disegno dello studio) adottati per rispettare il suo mandato di garante dei diritti dei malati. La tutela del paziente può dirsi garantita quando il CE abbia verificato che il trattamento sperimentale è la migliore opzione terapeutica a disposizione sia nel caso di malattie orfane sia nel caso di malattie con validi presidi terapeutici. Se così non fosse, ci troveremmo di fronte al paradosso inaccettabile di un paziente trattato con un farmaco sperimentale, la cui efficacia non è ancora dimostrata, negandogli di fatto l’accesso a terapie autorizzate perché di comprovata efficacia.
Esiste un’altra categoria di studi, i cosiddetti osservazionali, condotti sui farmaci autorizzati:
La tutela dei pazienti è quindi garantita a due livelli, dal codice deontologico medico[4], quando stabilisce la scelta di terapie di comprovata efficacia, e dal CE; ciò vale sia nell’uso clinico quotidiano, all’interno degli studi osservazionali e nell’uso sperimentale dei farmaci.
Se certamente tutto quanto sopra si applica ai medicinali ad uso umano, rimane un dubbio sulla tutela dei pazienti a cui i medici omeopati del Servizio Sanitario Nazionale prescrivono prodotti omeopatici: in Italia infatti nessun prodotto omeopatico è autorizzato con indicazione terapeutica approvata[5]; di conseguenza tutti dovrebbero essere considerati prodotti sperimentali ed il loro uso dovrebbe essere sottoposto al vaglio di un CE e al rilascio del consenso informato scritto da parte del paziente. L’uso del condizionale è obbligato visto che nella realtà ciò non avviene e i prodotti omeopatici “senza indicazioni terapeutiche approvate” (DL 2006/219) sono prescritti senza il secondo livello di tutela.
La difficoltà di sottoporre a sperimentazione clinica i prodotti omeopatici è ben comprensibile: viste le patologie in cui vengono di solito impiegati, il confronto con placebo sarebbe non eticamente percorribile perché non sarebbe etico trattare il gruppo di confronto con placebo negando al paziente il beneficio del farmaco efficace. Si dovrebbe quindi procedere ad un confronto verso farmaco efficace in quella specifica malattia; in questo caso il CE dovrebbe valutare la robustezza delle prove precliniche (laboratorio, su cellule e su animali) prima di avallare l’uso del prodotto omeopatico nell’uomo. Dato che queste prove precliniche mancano, nessun CE potrebbe concedere l’autorizzazione alla sperimentazione di confronto con farmaco efficace perché ciò implicherebbe trattare il gruppo dei pazienti con un prodotto omeopatico che non offre evidenze precliniche né di sicurezza né di ipotetica efficacia.
Nonostante ciò, i prodotti omeopatici sono usati nella pratica clinica di alcuni centri del Servizio Sanitario Nazionale e, in alcuni casi, in studi osservazionali che dovrebbero prevedere o la notifica o l’autorizzazione da parte di un CE. L’uso del condizionale è imposto dal fatto che molte pubblicazioni di studi osservazionali sui prodotti omeopatici non menzionano l’approvazione del CE e nemmeno l’utilizzo del consenso informato scritto.
Crediti immagini
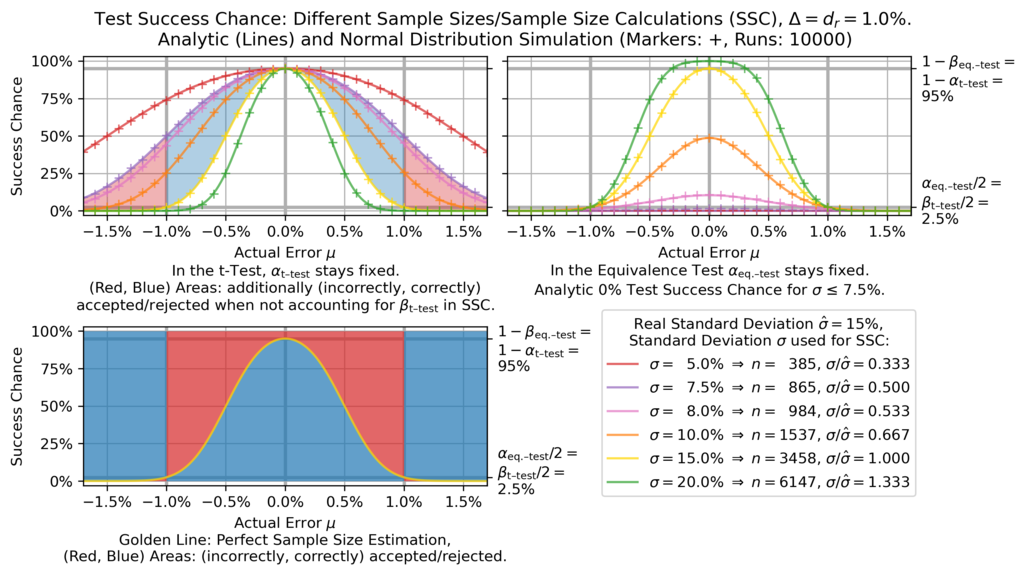
By Xor2k - Own work, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=79332746 https://commons.wikimedia.org/wiki/File:T-test_vs_equivalence_test.png#/media/File:T-te...
Tutelare le persone malate arruolate nella sperimentazione è compito dei Comitati Etici (CE) che intervengono nel processo di autorizzazione dello studio clinico.
Il Decreto legislativo 2003/211 (attuazione della direttiva 2001/20/CE relativa all’applicazione della buona pratica clinica nell’esecuzione delle sperimentazioni cliniche di medicinali per uso clinico”[2]) stabilisce che
il CE è “un organismo indipendente composto da personale sanitario e non, che ha la responsabilità di garantire la tutela dei diritti, della sicurezza e del benessere dei soggetti in sperimentazione e di fornire pubblica garanzia di tale tutela…”
Vediamo quali punti del protocollo sperimentale vengono valutati dal CE al fine di rispettare le responsabilità cui è chiamato per legge. Prima di tutto il CE valuta se le fasi precliniche e gli studi su volontari sani abbiano fornito evidenze solide di sicurezza e indicazioni di efficacia nell’uomo. A seguire si procede con l’analisi del protocollo sperimentale; il CE deve assicurare ai pazienti che il protocollo sia disegnato in modo appropriato per fornire dati validi e robusti. E’ evidente che non sia etico sottoporre le persone malate ad un trattamento in uno studio metodologicamente carente e che per questo non potrà fornire evidenze, cioè prove solide e credibili.
Per capire meglio l’impatto del disegno sperimentale sulla validità dei dati, procediamo con esempi partendo dai gruppi di pazienti in studio.
Allo scopo di verificare l’efficacia del farmaco A è necessario il confronto o con il placebo, cioè una sostanza inerte (zucchero o acqua, per esempio), o con un farmaco B di cui già se ne conosce l’efficacia. Se l’uso del placebo è eticamente accettabile quando la malattia su cui si conduce la sperimentazione è orfana, cioè non dispone di alcuna terapia approvata, al contrario, quando la patologia ha opzioni terapeutiche valide, il paragone andrà condotto verso il farmaco già registrato ed efficace nella specifica malattia. Quindi, lo studio deve essere controllato o verso placebo o verso altro farmaco efficace.
Altro elemento cruciale del disegno è l’analisi statistica: essa permette sia di calcolare il numero minimo di pazienti da arruolare a garanzia della robustezza delle conclusioni sia di stabilire, con una determinata certezza, la relazione tra l’efficacia e il farmaco in studio.
Le persone coinvolte devono essere adeguatamente informate su tutto ciò che riguarda il farmaco sperimentale, le procedure dello studio, i potenziali rischi e benefici. Solo un adeguato approfondimento di questi aspetti garantisce la libera scelta del paziente e il CE vaglia se il modulo del consenso informato scritto sia appropriato allo scopo.
Il CE deve, cioè, verificare la fattibilità del protocollo in termini di correttezza scientifica e coerenza tra obiettivi (dimostrare l’efficacia) e mezzi (disegno dello studio) adottati per rispettare il suo mandato di garante dei diritti dei malati. La tutela del paziente può dirsi garantita quando il CE abbia verificato che il trattamento sperimentale è la migliore opzione terapeutica a disposizione sia nel caso di malattie orfane sia nel caso di malattie con validi presidi terapeutici. Se così non fosse, ci troveremmo di fronte al paradosso inaccettabile di un paziente trattato con un farmaco sperimentale, la cui efficacia non è ancora dimostrata, negandogli di fatto l’accesso a terapie autorizzate perché di comprovata efficacia.
Esiste un’altra categoria di studi, i cosiddetti osservazionali, condotti sui farmaci autorizzati:
“Gli studi osservazionali sui farmaci sono di particolare importanza per la valutazione del profilo di sicurezza nelle normali condizioni di uso e su grandi numeri di pazienti, per approfondimenti sull’efficacia nella pratica clinica, per la verifica dell’appropriatezza prescrittiva e per valutazioni di tipo farmacoeconomico”[3]
Le linee guida per la classificazione e conduzione degli studi osservazionali stilate da AIFA, definiscono le caratteristiche degli studi osservazionali, cioè non sperimentali: “1.Il farmaco deve essere prescritto nelle indicazioni d’uso Autorizzate all’Immissione in Commercio in Italia; 2. La prescrizione del farmaco in esame deve essere parte della normale pratica clinica”[3]. Va sottolineato che, in funzione del tipo di studio osservazionale, le linee guida impongono o la notifica o la richiesta di autorizzazione al CE prima di procedere all’attuazione dello studio. La tutela dei pazienti è quindi garantita a due livelli, dal codice deontologico medico[4], quando stabilisce la scelta di terapie di comprovata efficacia, e dal CE; ciò vale sia nell’uso clinico quotidiano, all’interno degli studi osservazionali e nell’uso sperimentale dei farmaci.
Se certamente tutto quanto sopra si applica ai medicinali ad uso umano, rimane un dubbio sulla tutela dei pazienti a cui i medici omeopati del Servizio Sanitario Nazionale prescrivono prodotti omeopatici: in Italia infatti nessun prodotto omeopatico è autorizzato con indicazione terapeutica approvata[5]; di conseguenza tutti dovrebbero essere considerati prodotti sperimentali ed il loro uso dovrebbe essere sottoposto al vaglio di un CE e al rilascio del consenso informato scritto da parte del paziente. L’uso del condizionale è obbligato visto che nella realtà ciò non avviene e i prodotti omeopatici “senza indicazioni terapeutiche approvate” (DL 2006/219) sono prescritti senza il secondo livello di tutela.
La difficoltà di sottoporre a sperimentazione clinica i prodotti omeopatici è ben comprensibile: viste le patologie in cui vengono di solito impiegati, il confronto con placebo sarebbe non eticamente percorribile perché non sarebbe etico trattare il gruppo di confronto con placebo negando al paziente il beneficio del farmaco efficace. Si dovrebbe quindi procedere ad un confronto verso farmaco efficace in quella specifica malattia; in questo caso il CE dovrebbe valutare la robustezza delle prove precliniche (laboratorio, su cellule e su animali) prima di avallare l’uso del prodotto omeopatico nell’uomo. Dato che queste prove precliniche mancano, nessun CE potrebbe concedere l’autorizzazione alla sperimentazione di confronto con farmaco efficace perché ciò implicherebbe trattare il gruppo dei pazienti con un prodotto omeopatico che non offre evidenze precliniche né di sicurezza né di ipotetica efficacia.
Nonostante ciò, i prodotti omeopatici sono usati nella pratica clinica di alcuni centri del Servizio Sanitario Nazionale e, in alcuni casi, in studi osservazionali che dovrebbero prevedere o la notifica o l’autorizzazione da parte di un CE. L’uso del condizionale è imposto dal fatto che molte pubblicazioni di studi osservazionali sui prodotti omeopatici non menzionano l’approvazione del CE e nemmeno l’utilizzo del consenso informato scritto.
In conclusione, nelle sperimentazioni cliniche e negli studi osservazionali, la tutela dei diritti del malato passa anche attraverso il doppio livello di garanzia fornito dal codice deontologico medico[4] e dal vaglio del Comitato Etico[2][3], ciò è sicuramente vero per i farmaci registrati con efficacia clinica e indicazione approvata e dovrebbe esserlo anche per i prodotti omeopatici che in Italia sono tutti “senza indicazione terapeutica approvata”[5].
L’uso dei prodotti omeopatici prescritti all’interno del Servizio Sanitario Nazionale pur se legittimo, avallato cioè dalle competenti amministrazioni regionali con appositi atti, non definisce l’efficacia dei rimedi, mai provata da studi registrativi di efficacia, e sottrae il paziente alla tutela garantita dalla verifica del Comitato Etico in caso di sperimentazioni o studi osservazionali. Crediti immagini
By Xor2k - Own work, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=79332746 https://commons.wikimedia.org/wiki/File:T-test_vs_equivalence_test.png#/media/File:T-te...
Biografia dell’autrice: Laureata in Medicina e Chirurgia, specializzata in Psichiatria e Master in Patologia Genetico Molecolare. Ha esperienza pluriennale come medico di base, come Psichiatra e nella sperimentazione clinica di farmaci e vaccini. Si veda il profilo Linkedin per maggiori dettagli
Bibliografia 2) Decreto legislativo 24 giugno 2003, n. 211. Attuazione della direttiva 2001/20/CE relativa all’applicazione della buona pratica clinica nell’esecuzione delle sperimentazioni cliniche di medicinali per uso clinico. Gazzetta Ufficiale della Repubblica Italiana – Serie generale 9 agosto 2003, n. 184 (supplemento ordinario n. 130).